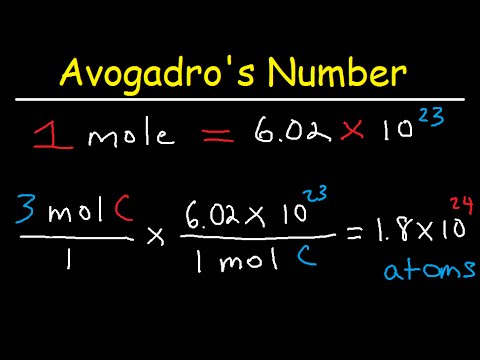
Contenu

En chimie, une mole représente un grand nombre d'atomes, de molécules ou d'autres particules microscopiques. Dans le cas de la conversion d'atomes en moles, une mole contient 6,022 x 10 ^ 23 atomes. Les grains de beauté ont également une autre propriété utile: une mole de toute substance a une masse en grammes égale au poids moléculaire de la substance. Armé de la connaissance des propriétés de la taupe et d'un tableau périodique, vous pouvez convertir des atomes en molécules pour des grammes de toute substance.
Étape 1
Divisez le nombre d'atomes par le nombre d'Avogadro, 6,022 x 10 ^ 23, pour trouver le nombre de moles. Si vous avez 5 x 10 ^ 24 atomes d'azote, par exemple, divisez-le par 6,022 x 10 ^ 23 pour obtenir 8,3 moles d'azote.
Étape 2
Recherchez l'élément dans le tableau périodique et vérifiez le nombre sous le symbole de l'élément en grammes par mol pour obtenir le poids moléculaire. Le symbole de l'azote est N, par exemple, et le nombre sous N dans le tableau périodique est 14,0067, donc le poids moléculaire de l'azote est 14,0067 g / mol.
Étape 3
Multipliez le poids moléculaire par le nombre de moles pour obtenir la masse. Pour 8,3 moles d'azote, multipliez-le par 14,0067 g / mol pour obtenir 116,26 g d'azote.